Sølvklorid
| Sølvklorid | |
|---|---|
| Generelt | |
| Systematisk navn | Sølv(I)klorid |
| Molekylformel | AgCl |
| Molarmasse | 143,32 g/mol |
| Fremtræden | Hvide krystaller |
| CAS-nummer | |
| SMILES | [Ag+].[Cl-] |
| Kemiske egenskaber | |
| Massefylde | 5,56 g/cm3 |
| Opløselighed i vand | 5,2 × 10-3 g/100 ml ved 50 °C |
| Smeltepunkt | 457 °C |
| Kogepunkt | 1547 °C |
| Sikkerhed | |
| NFPA 704 | |
| LD50 | >5110 mg/kg |
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |
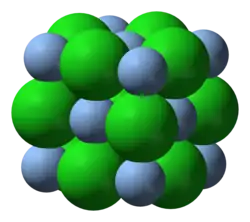

Egenskaber
Lysfølsomhed
Sølvklorid er følsomt for lys og nedbrydes til metallisk sølv og klorgas når det udsættes for lys.
Opløselighed i vand
Sølvklorid er særdeles sværtopløseligt i vand. Ved at dryppe en sølvnitratopløsning i en prøve, kan man påvise kloridioner ved at der opstår et uklart bundfald af sølvklorid:
Opløselighed i ammoniak
Til gengæld opløses sølvklorid let i ammoniak og danner sølvdiammin- og kloridioner
Anvendelse
- På grund af lysfølsomheden anvendes sølvklorid i fotografiske sammenhænge, eksempelvis i fotopapir.
- Samme egenskab udnyttes i fotokromatiske linser, f.eks. i briller.
- Sølvklorid bruges også i behandlingen af kviksølvforgiftning.
| Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
